惠连健康
普惠全民健康.连通全球医药
手机号 13225168454 微信hldydg












氘可来昔替尼的简明处方信息
【名称】
通用名称:氘可来昔替尼片
商品名称:Sotyktu
英文名称:Deucravacitinib
【适用症】
用于全身治疗或光疗中度至重度斑块状银屑病的成人患者。
Sotyktu不建议与其他强效免疫抑制剂联合使用。
【规格】
片剂,6mg。
【用法用量】
推荐剂量为每天一次口服6毫克,有或没有食物。
【禁忌】
已知对Deucravacitinib或Sotyktu中的任何赋形剂过敏。
【贮藏】
将Sotyktu片剂存放在20°至25°C;允许在15°和30°C之间偏移。
【银屑病氘可来昔替尼购买咨询】请咨询手机号13225168454 微信号 hldydg 全体24小时服务。
【治疗现状】
银屑病
银屑病(牛皮癣)是一种广泛流行的、慢性、系统性免疫介导疾病,严重影响患者的身体健康、生活和工作,全球至少有1.25亿人受此疾病困扰。
根据银屑病的临床特征,可分为寻常型、脓疱型(局限性和泛发性两型)、红皮病型及关节病型(又称为银屑病性关节炎),其中90%以上为寻常型。而寻常型银屑病可分为点滴状和斑块状两型,其中,斑块状银屑病是最常见的一种,大约占80%-90%。
银屑病的现有治疗方案主要是对症治疗,且不少患者需要长期医治,而各种疗法都有一定的不良反应,同时,仍有许多中重度银屑病患者未得到充分治疗。因此,临床急需创新治疗手段。而氘可来昔替尼则为中重度斑块型银屑病患者群体带来一种受欢迎的新一线口服治疗方案,是近10年来全球首款获批上市的中度至重度斑块状银屑病口服治疗药物。
【氘可来昔替尼治疗中重度斑块状银屑病的疗效和安全性】
2022年9月10日,百时美施贵宝(BMS)宣布,其TYK2抑制剂氘可来昔替尼(deucravacitinib)治疗斑块状银屑病的上市申请已获FDA批准,商品名为Sotyktu。氘可来昔替尼是全球首款获批上市的TYK2抑制剂,国家药品监督管理局也于7月15日受理该药物的上市申请。
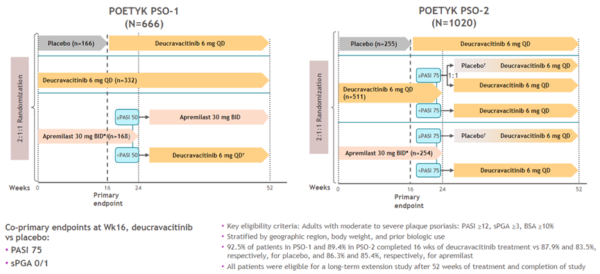
III期临床试验:POETYK PSO-1、POETYK PSO-2
内容:两项试验均为全球性、多中心、双盲、随机、安慰剂和阳性药物对照研究,分别纳入了666例患者和1020例患者,旨在评估氘可来昔替尼对比阿普米司特(apremilast)和安慰剂治疗中重度斑块状银屑病成人患者的疗效和安全性。
共同的主要终点:第16周时银屑病面积与严重性指数(PASI)评分改善75%以上和sPGA 0/1(静态医生总体评估皮肤症状完全清除/几乎完全清除)的患者比例。
结论:第16周时,与安慰剂组和阿普米司特组相比,氘可来昔替尼组PASI评分改善75%以上(58.7%)和sPGA 0/1的患者(53.6%)比例显著增加。试验还达到了所有次要终点,氘可来昔替尼在症状负担和生活质量测量值上表现出显著且具有临床意义的改善。此外,氘可来昔替尼耐受性良好,因不良事件导致的停药率低。
【氘可来昔替首个以中国为主的亚洲多中心临床研究】
研究内容
POETYK PSO-3是氘可来昔替尼(Deucravacitinib)首个以中国为主的亚洲多中心银屑病III期临床研究。POETYK PSO-3是一项多中心、随机、双盲、安慰剂对照的III期临床研究,POETYK PSO-3研究共入组220位中重度斑块状银屑病亚洲患者,其中81.8%为中国患者。入组患者随机接受氘可来昔替尼(Deucravacitinib)或安慰剂治疗至第16周,之后所有受试患者继续以盲态形式接受氘可来昔替尼(Deucravacitinib)治疗至第52周。
研究目的
旨在评估氘可来昔替(Deucravacitinib)(6 mg,口服,每日一次)对比安慰剂治疗亚洲中重度斑块状银屑病患者的有效性和安全性。
安全性
POETYK PSO-3研究中氘可来昔替(Deucravacitinib)的总体安全性与耐受性良好,与全球关键III期POETYK PSO-1 和POETYK PSO-2研究安全性特征一致。不良事件以轻度或中度为主,最常见不良事件(>10%)为上呼吸道感染和鼻咽炎,未观察到新的安全信号。研究中未报告死亡、肿瘤、重大心血管不良事件、机会性感染、血栓及自杀意念及行为等事件。
研究结果
在所有随机分组至氘可来昔替尼(Deucravacitinib)治疗组的患者中:
68.8%的患者在第16周达到PASI 75(银屑病面积和严重程度指数改善至少75%),优于安慰剂组(8.1%,P<0.0001);38.2%的患者达到PASI 90(银屑病面积和严重程度指数改善至少90%,即皮损几乎清除),优于安慰剂组 (1.4%,P<0.0001);
持续接受deucravacitinib治疗到第52周时,PASI 75应答率保持稳定,PASI 90应答率则进一步提升至45.5%。
尤其值得一提的是,deucravacitinib对于难治部位(头皮)的皮损清除也显示出显著获益,62.9%罹患中重度头皮银屑病的患者在持续接受16周deucravacitinib治疗后达到ss-PGA 0/1(头皮皮损清除或基本清除),优于安慰剂组(9.8%,P<0.0001)。
【服用氘可来昔替尼的注意事项】
超敏反应:已经报道了血管性水肿等超敏反应。如果发生临床上显着的超敏反应,请停止使用。
感染:SOTYKTU可能会增加感染风险。避免在有活动性或严重感染的患者中使用。如果发生严重感染,请停止SOTYKTU直至感染消退。
结核病:在开始使用SOTYKTU治疗之前评估结核病。
恶性肿瘤:在SOTYKTU(deucravacitinib)的临床试验中观察到包括淋巴瘤在内的恶性肿瘤。
横纹肌溶解症和CPK升高。
实验室异常:定期评估血清甘油三酯。在基线和之后评估已知或疑似患者的肝酶,肝病。
免疫:避免与活疫苗一起使用。
与JAK抑制相关的潜在风险:目前尚不清楚TYK2抑制是否与观察到的或潜在的JAK抑制不良反应有关。
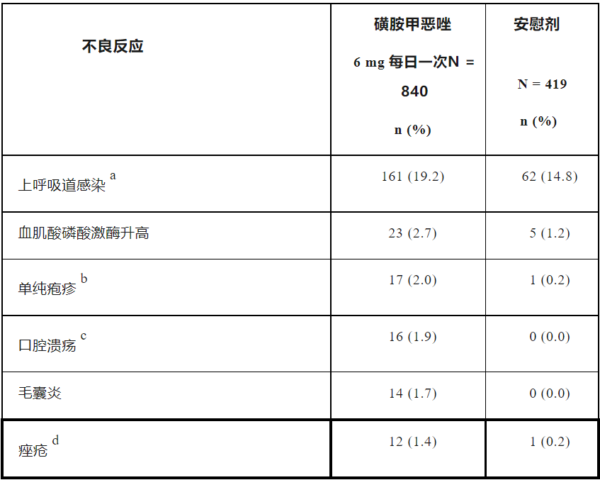
【服用氘可来昔替尼的不良反应】
临床试验中,不良事件(AE)以轻度或中度为主,最常见的 AE(≥10%)为鼻咽炎、上呼吸道感染和头痛。
严重 AE 和导致停药的 AE 在长达两年内保持较低水平,未观察到新的安全性信号,未观察到新的安全信号。研究中未报告死亡、肿瘤、重大心血管不良事件、机会性感染、血栓及自杀意念及行为等事件。
氘可来昔替尼耐受性良好,因不良事件导致的停药率低。
Deucravacitinib 目前在 ClinicalTrials.gov 共登记有 50 多项临床试验。除银屑病外,也在拓展红斑狼疮、克罗恩病、溃疡性结肠炎等适应症。在国内,针对克罗恩病、狼疮性肾炎的研究已进入 II 期临床阶段。
| 重量 | 0.5 公斤 |
|---|---|
| 【名称】 | 通用名称:氘可来昔替尼片 |
| 【适用症】 | 用于全身治疗或光疗中度至重度斑块状银屑病的成人患者。 |
| 【规格】 | 片剂,6mg。 |
| 【用法用量】 | 推荐剂量为每天一次口服6毫克,有或没有食物。 |
| 【贮藏】 | 将Sotyktu片剂存放在20°至25°C;允许在15°和30°C之间偏移。 |
| 【银屑病氘可来昔替尼购买咨询】 | 请咨询手机号13225168454 微信号 hldydg 全体24小时服务。 |
评价
目前还没有评价